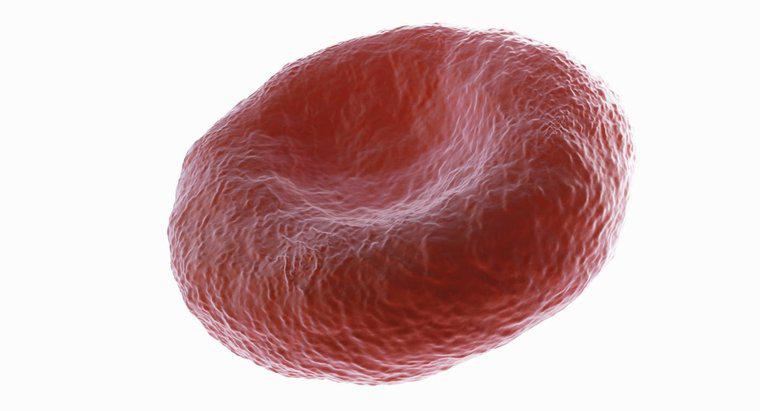
Lorsque les globules rouges sont placés dans de l'eau distillée, qui est hypotonique par rapport à la solution contenue dans les membranes des cellules, l'eau distillée va diffuser dans les globules rouges et les faire éclater. Placer des globules rouges dans n'importe quelle solution qui contient un degré de soluté inférieur à celui de la solution à l'intérieur des cellules provoquera la diffusion d'eau dans celles-ci. Parce que l'eau distillée contient une concentration nulle de soluté, elle diffusera de manière prévisible dans un globule rouge pour tenter d'égaliser la pression osmotique des deux côtés de la membrane cellulaire.
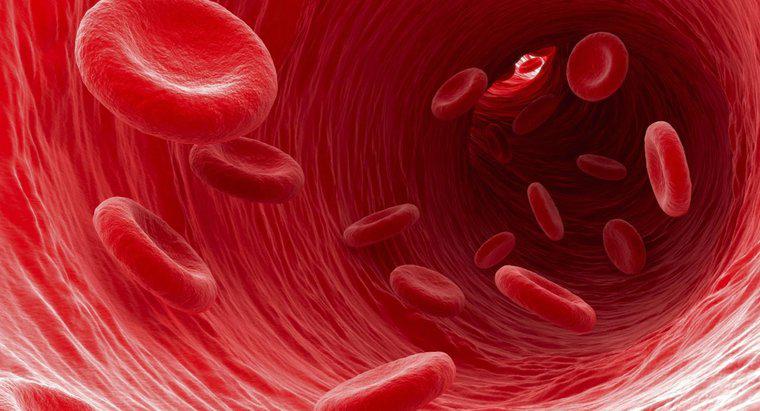
Dans un organisme sain, les globules rouges sont capables de conserver leur forme et ne se dilatent ni n'éclatent dans la circulation sanguine, car la pression osmotique à l'intérieur de la cellule est égale à la pression osmotique du sérum sanguin qui l'entoure. Cet équilibre de la pression osmotique est appelé isotonicité. Si le sérum dans la circulation sanguine contenait une concentration de soluté moindre que la solution contenue dans les globules rouges, cela rendrait le sérum hypotonique. La pression osmotique inégale provoquerait alors la diffusion de la partie eau du sérum sanguin dans les globules rouges, provoquant leur gonflement.