Comme tous les métaux alcalino-terreux, le magnésium a deux électrons de valence, ce qui signifie qu'il y a deux électrons dans sa couche externe. Les électrons de valence sont ceux qu'un atome partage, gagne ou perd lorsqu'il interagit avec d'autres atomes.
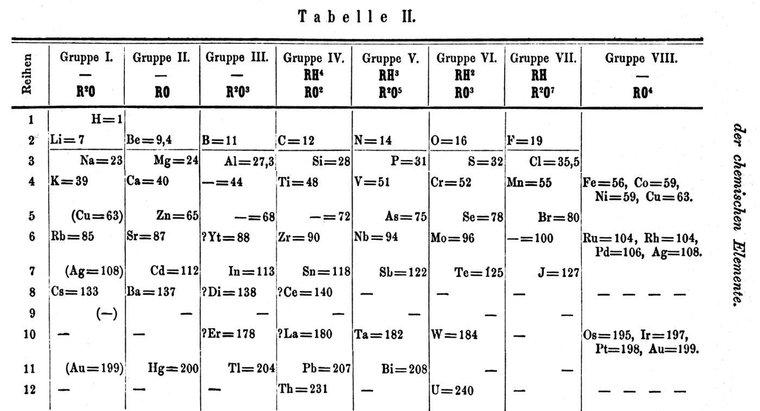
Les métaux alcalino-terreux constituent le groupe IIA du tableau périodique des éléments. Le magnésium, comme les autres métaux alcalino-terreux, est plus susceptible de perdre ses deux électrons lorsqu'il réagit avec d'autres atomes, formant ainsi des cations divalents. Cela est dû au fait que les électrons n'ont pas de lien fort avec le noyau. Le magnésium a également un faible niveau d'affinité électronique et une faible électronégativité. Le magnésium a un numéro atomique de 12.