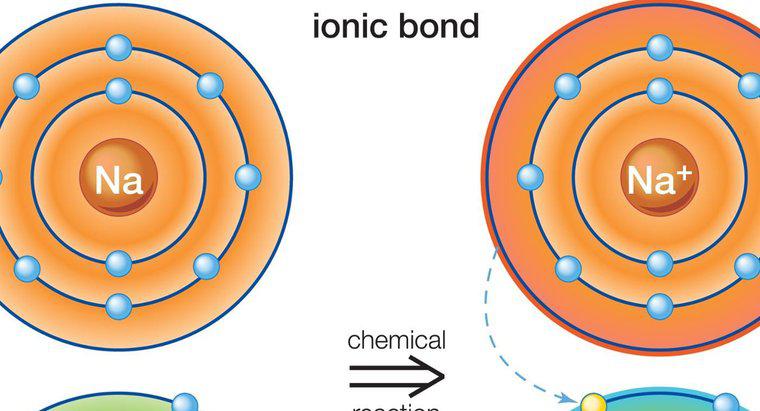
Les composés ioniques sont électriquement neutres car les charges des cations et des anions qui le composent s'annulent. Dans le cas du sel par exemple, le sodium a une charge positive, et le chlorure a une charge négative. Ensemble, ils neutralisent le composé.
Les composés ioniques sont constitués d'atomes ou de molécules chargés positivement et négativement. Ceux avec une charge positive sont appelés cations, tandis que ceux avec une charge négative sont appelés anions. Les deux sont attirés l'un par l'autre en raison de leurs charges opposées. Les cations et les anions peuvent attirer plus d'une molécule du type opposé, créant une molécule plus longue maintenue ensemble par des liaisons ioniques.
Le chlorure de calcium est un autre exemple de composé ionique, le calcium positif annulant le chlorure négatif. Le bromure de fer fait de même, la charge positive du fer annulant la charge négative du bromure. Cette neutralité électrique aide à garder le composé stable, le rendant plus facile à travailler et beaucoup moins volatil que les ions instables.
La plupart des composés ioniques sont des solides avec des points de fusion élevés. Ils sont souvent formés d'un élément métallique et d'un élément non métallique. Les composés fabriqués à partir de deux non-métaux sont souvent des composés liés par covalence.