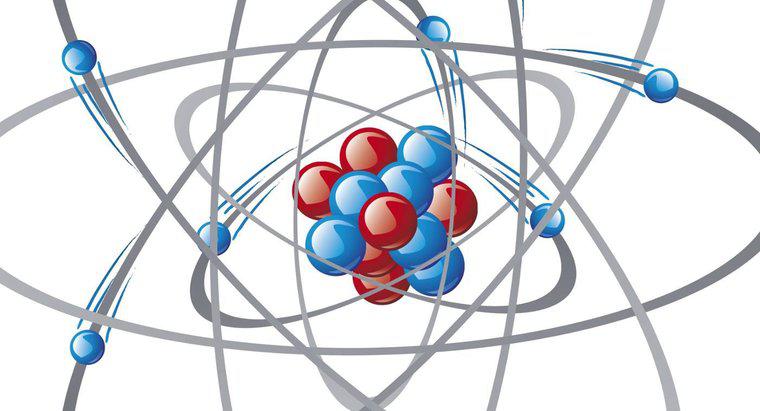
Le nuage d'électrons est un moyen de visualiser les résultats des équations mathématiques utilisées pour calculer la position d'un électron en orbite autour du noyau de l'atome. La zone où le nuage est le plus dense décrit le plus emplacement probable de l'électron à un moment donné.
Les scientifiques utilisent de nombreux modèles d'atomes différents pour comprendre leur comportement et leur interaction avec d'autres matériaux. Le modèle de Bohr de 1913 décrit l'atome comme des cercles concentriques d'orbitales électroniques chargées négativement entourant le noyau chargé positivement, mais est incapable d'expliquer les résultats expérimentaux d'Erwin Schrödinger en 1926 sur le tir de particules chargées à travers une fente dans une feuille d'or. Le modèle de nuage d'électrons, avec des électrons capables de se déplacer à travers des orbitales avec des énergies et des formes caractéristiques, offre un meilleur ajustement pour les données expérimentales. L'équation de Schrödinger, avec une infinité de solutions, prédit à la fois la forme et la densité du nuage. Le modèle prend également en compte le principe d'incertitude de Heisenberg. Le modèle de nuage d'électrons, ainsi que le modèle de Bohr, considère les atomes comme constitués uniquement de particules chargées positivement et négativement. La découverte du neutron en 1932 a conduit à un raffinement supplémentaire du modèle. Depuis 1932, les scientifiques continuent de découvrir des particules supplémentaires dans l'atome, entraînant des changements dans les descriptions atomiques.