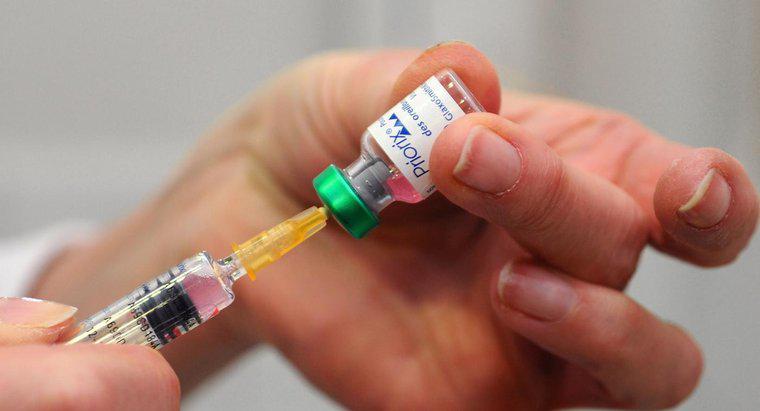
Une application pratique de la loi de Boyle consiste à aspirer du liquide dans une seringue. Tirer sur le piston augmente le volume intérieur de la seringue et réduit sa pression. Le fluide à l'extérieur de la seringue est aspiré dans le cylindre jusqu'à ce que les pressions intérieure et extérieure soient équilibrées.
La loi de Boyle stipule que le volume et la pression d'un gaz ou d'un liquide restent constants à condition que la température de la substance reste la même. Cette loi, qui a été déclarée pour la première fois par Robert Boyle au 17ème siècle, est d'une importance vitale dans les applications d'ingénierie telles que la conception de moteurs. Sa formule est V1/V2=P2/P1 (à température constante), où V1 est le volume initial, V2 est le volume modifié, P1 est la pression de départ et P2 est la pression modifiée.
La loi la plus étroitement liée à la loi de Boyle est la loi de Charles, ou la "loi des volumes", qui est l'œuvre du scientifique français Jacques Charles. Il décrit la relation entre le volume et la température. La loi de Boyle et la loi de Charles sont toutes deux des théories des gaz qui décrivent le comportement d'un gaz "idéal" hypothétique. Dans la pratique, cependant, les deux s'appliquent également aux liquides. La loi de Boyle est parfois appelée loi de Mariotte, en référence au chercheur français qui a découvert les mêmes principes 14 ans après la publication de Boyle. Cette convention de nommage est populaire en France et dans d'autres pays européens.