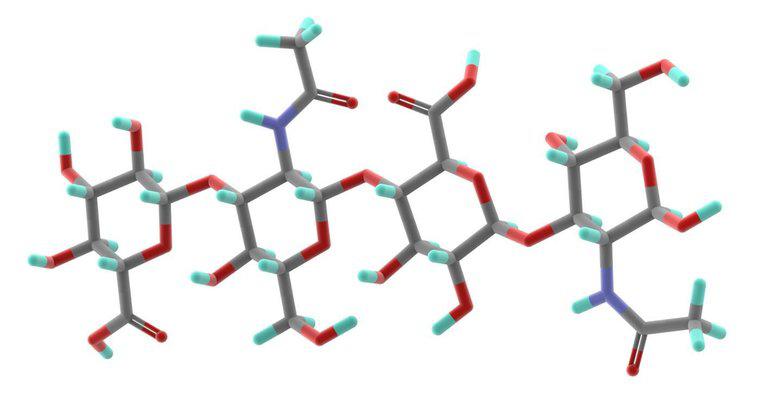
Chaque atome de carbone forme quatre liaisons chimiques. Le carbone forme le plus souvent des liaisons covalentes, qui sont deux atomes partageant des électrons, mais forme aussi parfois des liaisons ioniques présentes dans des composés, tels que le carbure de calcium.
Le carbone a six électrons : deux sur l'orbite interne et quatre sur l'orbite externe. L'orbite extérieure est terminée lorsqu'elle atteint huit électrons, et les atomes de carbone forment donc des liaisons covalentes avec d'autres atomes avec des électrons à partager. Bien que le carbone ne soit pas le seul élément à quatre électrons de valence, ou électrons externes, il est le plus petit, ce qui lui permet de s'intégrer confortablement dans des molécules beaucoup plus grosses.
Tout composé contenant du carbone lié de manière covalente est considéré comme un composé organique. Plus de 10 millions de composés organiques sont connus des chimistes, qui en synthétisent toujours plus. La capacité du carbone à former des chaînes carbone-carbone est l'une des raisons pour lesquelles le carbone peut former autant de composés. Les atomes de carbone peuvent former des chaînes, des branches complexes et des anneaux. Le carbone se lie aux éléments en partageant un, deux ou trois électrons, ce qui lui permet de se lier à un large éventail d'autres atomes. L'hydrogène est l'élément le plus courant pour se lier au carbone, mais l'azote, l'oxygène, le phosphore, le soufre et les halogènes, ainsi que de nombreux autres types d'atomes, se lient au carbone pour former des molécules organiques.