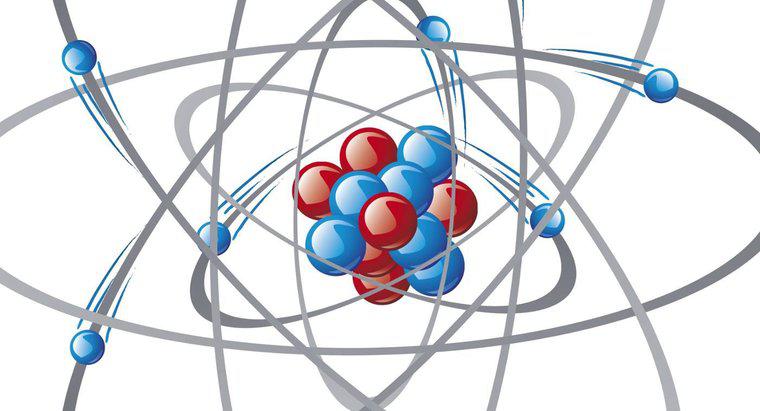
Un ion chlorure a 18 électrons au total. L'ion chlorure a un électron supplémentaire pour compléter la couche électronique la plus externe, ou couche de valence, de l'atome.
Le chlore est un élément hautement réactif, en raison de la couche externe d'électrons. Les électrons remplissent les anneaux, appelés coquilles, à l'extérieur de l'atome. La première couche, la plus proche de l'atome, contient deux électrons. Chaque coquille après cette coquille initiale contient jusqu'à huit électrons, et chaque atome a des anneaux pour accueillir tous les électrons, mais pas plus. Le chlore a 17 électrons; par conséquent, le premier anneau est rempli de deux électrons, le deuxième anneau est rempli de huit électrons, mais il n'y a que sept électrons pour le troisième anneau. Cela rend la couche de valence du chlore incomplète et l'atome attire des électrons "libres" vers cette couche pour la compléter, de sorte que l'atome peut être stable. Le chlorure est un atome de chlore, qui a trouvé ce dernier électron et l'a ajouté à la couche de valence la plus externe pour devenir stable. Cet électron ajouté donne à l'ion chlorure une charge négative et est donc considéré comme un anion.