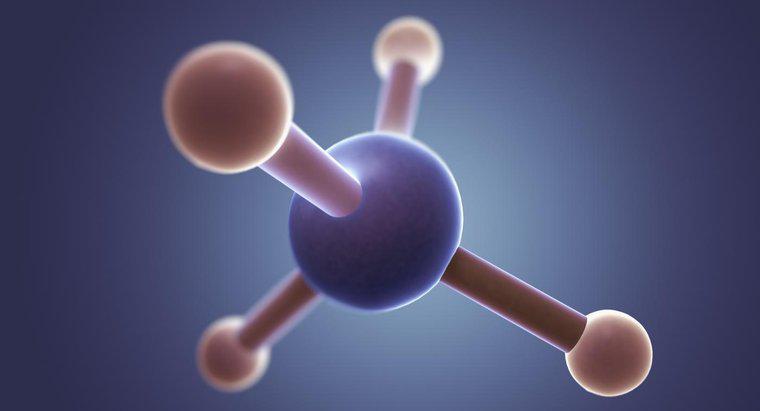
La structure de Lewis de C2Cl4 comprend une chaîne à deux carbones à double liaison avec deux atomes de chlore attachés à chaque atome de carbone. À chaque extrémité, les atomes de chlore sont espacés d'environ 120 degrés les uns des autres et de l'atome de carbone.
C2Cl4 est le tétrachloroéthylène selon le système de dénomination systématique, mais son nom commun est perchloroéthylène. Le perchloroéthylène est un solvant de nettoyage à sec courant. Comme le montre sa structure de Lewis, il est non polaire, ce qui en fait un solvant idéal pour de nombreux autres matériaux organiques non polaires. Le fait qu'il soit ininflammable et très stable en fait un composé préféré pour une utilisation par les nettoyeurs à sec. Le solvant agit sur les huiles et les graisses, ce qui le rend populaire pour le nettoyage des métaux.
C2Cl4 dissout les graisses dans les tissus humains. Il élimine les graisses de la peau, provoquant dessèchement et irritation. Il est facilement absorbé par les poumons. Les problèmes de santé liés au C2Cl4 ont conduit de nombreux nettoyeurs à sec à rechercher un solvant plus sûr pour leurs utilisations. L'EPA classe le tétrachloroéthylène comme un cancérogène probable. C'est un irritant respiratoire et provoque des problèmes de reproduction. L'exposition à long terme à des personnes travaillant dans l'industrie du nettoyage à sec peut entraîner des problèmes de capacités cognitives et motrices. Lorsqu'il est libéré dans l'atmosphère dans l'hémisphère nord, la plupart du C2Cl4 reste dans l'air et sa dégradation nécessite jusqu'à 5 mois.