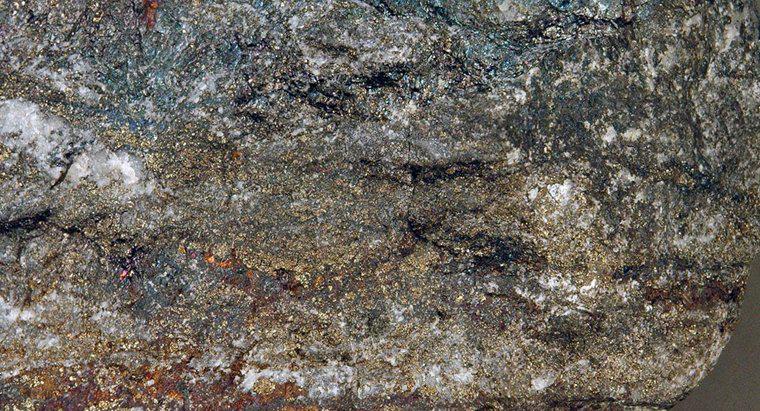Les solides sont définis comme des substances qui conservent leur forme, même lorsqu'elles ne sont pas confinées. Les substances assument généralement l'état solide d'être à des températures plus basses que lorsqu'elles sont liquides, gazeuses ou plasmas.
Par exemple, un morceau de glace conserve sa forme même lorsqu'il n'est pas dans un récipient. Cependant, si la température augmente, la glace commencera à fondre et à se transformer en liquide. Les liquides ne conservent pas leur forme lorsqu'ils sont à l'extérieur d'un récipient, de sorte que l'eau aura tendance à s'échapper de la glace. Si la température se réchauffe encore plus, l'eau prendra la forme d'un gaz. Les gaz ont encore moins de forme que les liquides, et le gaz peut même monter dans l'air.
De nombreux éléments sont naturellement présents à l'état solide, notamment l'or, le carbone, le sodium et l'argent. Cependant, le terme « solide » s'applique à la fois aux produits chimiques purs ainsi qu'aux composés et mélanges. Par exemple, l'eau se présente sous la forme des trois principales formes de matière à différents endroits du monde. La forme solide de l'eau, également connue sous le nom de glace, se produit dans des endroits où la température est suffisamment froide pour que les molécules se déplacent très étroitement ensemble et se bloquent en place.
Certains solides présentent une structure cristalline au niveau moléculaire. Cela confère à certains de ces matériaux, comme les diamants, une résistance remarquable. Cependant, de nombreux solides cristallins sont sujets à la fracturation le long d'un seul plan ou d'une seule surface.