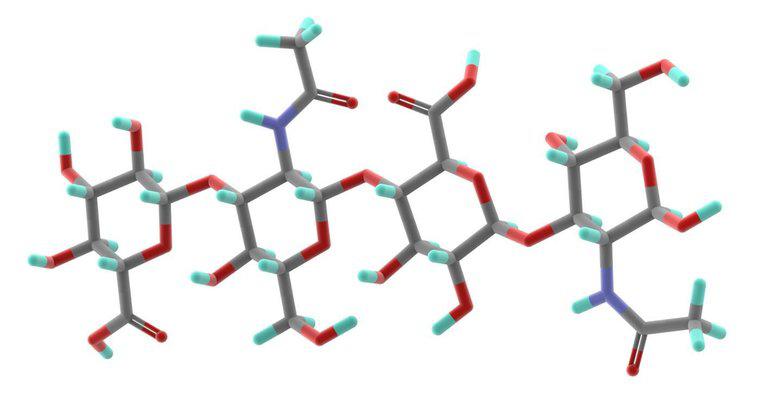
La dissolution est la dissociation ou l'occupation intermoléculaire d'une espèce de soluté dans une espèce de solvant pour former une solution. Un processus de dissolution courant est l'introduction de cristaux de sel de table dans l'eau pour former une solution d'eau salée.
Une règle générale de dissolution est que "le semblable dissout le semblable". Les substances doivent posséder des forces intermoléculaires similaires pour pouvoir se dissoudre les unes dans les autres. L'introduction d'un soluté dans un solvant doit impliquer une certaine interaction entre les deux espèces pour qu'une solution se forme.
Pour un soluté solide se dissolvant dans un solvant liquide, les interactions entre les molécules du soluté et le solvant doivent être plus fortes que les interactions entre les molécules de solvant. Plus ces interactions sont fortes, plus le soluté se dissout rapidement dans le solvant et plus la quantité de soluté que la même quantité de solvant est capable de dissoudre est importante.
Un exemple est la dissolution de sels fortement ioniques dans des solvants polaires, tels que l'eau. Les molécules d'eau sont capables de séparer les molécules de soluté en ions individuels et de les entourer pour former une solution. Ce mécanisme consistant à entourer les molécules de soluté de molécules de solvant est appelé solvatation et doit se produire quelles que soient les phases impliquées pour qu'une solution se forme.